在过去几十年中,过渡金属催化的不对称交叉偶联取得了巨大的成就。镍催化剂由于其特殊的催化活性,被广泛用于该领域的研究。虽然在C(sp2)-C(sp3)偶联方面已经有了长足的发展,但是镍催化的对映体选择性C(sp3)-C(sp3)偶联构建仍然极具挑战性。已有的研究报道大多使用烷基有机金属试剂,不过其对空气和水敏感,使得其官能团兼容性相对较差。随后又陆续发展了一些NiH催化的方法,但两个烷基卤化物的对映选择性还原交叉偶联仍然是有待解决的难题。
近日,我院徐涛教授课题组使用α-氯代硼酸酯和未活化的烷基碘化物作为原料,利用光/镍协同催化还原交叉偶联的策略,实现了该C(sp3)-C(sp3)键的手性构建,得到了一系列手性二级烷基硼酸酯化合物。相关成果“Enantioselective C(sp3)-C(sp3) Reductive Cross-Electrophile Coupling of Unactivated Alkyl Halides with α-Chloroboronates via Dual Nickel/Photoredox Catalysis” 在线发表于化学领域国际知名学术期刊《美国化学会志》(Journal of the American Chemical Society)上。

在最优条件下,研究人员对反应的适用范围进行了考察。结果表明,反应对各类官能团如酯、醚、氰基、磺酰胺、三氟甲基、酰胺、烷基氯化物以及多种天然产物衍生物等均有很好的兼容性。除此之外,二级碘化物在该反应中也能兼容。温和的反应条件也使得该方法用于复杂分子的后期修饰成为可能。研究人员还对反应的机理进行了深入的探讨,提出了可能的反应循环。
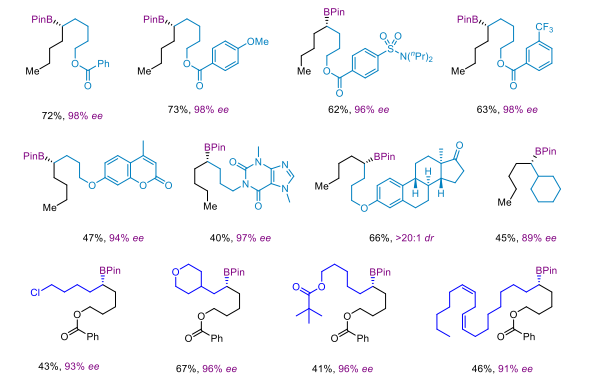
这项研究工作发展了一种全新的光/镍催化还原交叉偶联构建C(sp3)-C(sp3)键的策略。这种策略利用易获得的烷基碘化物作为反应原料,具有许多显著的优点,如温和的反应条件、良好的底物范围和显著的官能团兼容性。更为重要的是用于镍催化的传统还原剂不能有效实现这种转化,进一步体现了这种双催化体系的巨大优势,为后续其他手性C(sp3)-C(sp3)键偶联反应提供了新的研究思路。
我院硕士研究生周珺为论文第一作者,徐涛教授为通讯作者。研究工作得到了国家自然科学基金等项目的资助。
论文链接:https://pubs.acs.org/doi/10.1021/jacs.2c13220
