丰富的海水资源可能成为太阳能燃料制备的重要反应底物 我系陈作锋课题组研究成果在《J.Am. Chem. Soc.》上发表 近日,我系陈作锋教授课题组作为主要完成人的研究成果“A half-reaction alternative to water oxidation: chloride oxidation to chlorine catalyzed by silver ion”发表在国际知名杂志《J. Am. Chem. Soc.》(2015,137(9), 3193–3196)上。《J. Am. Chem. Soc.》是目前国际化学领域最具影响力的综合性刊物之一,该刊物最新影响因子为11.4。 通过太阳光驱动化学反应制备化学燃料(即太阳能燃料)是太阳能转化和利用的一种重要方式。水氧化反应(2H2O → O2+ 4H++ 4e–,Eo= 1.23 V vs. NHE)是其中的重要半反应,为CO2、质子/水还原半反应提供质子和还原当量。然而水氧化具有高度的复杂性和困难性,反应涉及两分子水结合形成O-O键,同时伴随着失去4个电子和4个质子。氯离子氧化生成氯气(2Cl–→ Cl2+ 2e–,Eo= 1.36 V)可视作潜在的水氧化替代半反应。海水中富含氯,氯离子是海水的主要成分之一。氯离子氧化相对水氧化具有如下一些显著优点:氯离子氧化生成氯气(∆G= 2.72 eV)比水氧化生成氧气(4.92 eV)能量低45%;在光电催化的应用中,前者只需2个光子驱动即可完成(即两电子氧化),而后者则需4个光子;虽然Cl2/Cl–电对的标准电极电位(1.36 V vs. NHE)比O2/H2O电对(1.23 V)高出130 mV,氯离子氧化可避免水氧化过程中高能过氧化物中间体的生成;此外,氯离子氧化生成氯气不涉及质子,反应过程相对简单。氯离子氧化同时也是氯碱工业生产中的重要半反应,因此开发高效、稳定的氯离子氧化催化剂对氯碱工业也具有重要意义。目前氯离子氧化分子催化剂鲜有文献报道。 在高浓度的氯化物溶液中,Ag(I) 以可溶性AgCl2–和AgCl32–配合物的形式存在。该项研究巧妙地利用这一现象,将Ag(I) 潜在的催化活性(通过氧化到高价态)和氯离子的配位作用相结合,实现高效的氯离子催化氧化。Cl–的配位作用除避免Ag(I) 生成AgCl沉淀外,其对中心金属氧化电荷的离域分散作用,极大地降到了达到高价银所需电位。与Ag2+/+的标准电极电位(1.98 V)相比,AgCl2–和AgCl3−催化氯离子氧化生成氯气的起始电位为1.37 V,降低了约600 mV;同时,与Cl2/Cl–的电极电位(1.36 V)相比,氯离子氧化过电位仅10 mV。催化效率高,仅微摩尔量的Ag(I) 即可获得2 mA/cm2的氯离子氧化电流;催化性能稳定,不存在有机配体引起的催化剂分解的问题。机理研究显示,由于氯离子的配位作用,有效地避免了中心金属在连续氧化过程中的电荷累积和高能量中间体的生成,使得反应的热力学驱动力更加有利(如下图)。该项研究有可能使得丰富的海水资源成为太阳能燃料制备的重要反应底物。 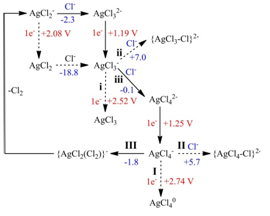
Ag(I) 催化氯离子氧化生成氯气的反应机理(实线为可能机理) bat365在线平台校园新闻网链接 |
